荧光大环分子因其独特的发光性能和可调控的多功能性,一直是新材料和生物医药研究领域的热点之一。它们不仅能用于荧光成像,还在药物递送和疾病诊疗等方面展现出广阔的应用前景。开发可调控其在光照条件下产生活性氧(ROS)能力的新技术变得尤为重要,因为ROS正是光动力抗菌和治疗中的关键活性因子。
近日,海角社区
杨英威教授课题组联合天津工业大学高辉教授课题组成功合成了一类新型三联苯拓展柱[6]芳烃,并通过引入苯并噻二唑单元,构建出具有聚集诱导发光增强特性的荧光大环化合物。进一步研究发现,季铵盐功能化的大环在光照下表现出显著提升的单线态氧生成能力,并可与抗生素头孢唑肟钠协同作用,有效增强抗菌效果。研究成果以“Macrocycle Formation-Mediated Augmentation in Reactive Oxygen Species Production”为题发表在《Chemical Science》(DOI:10.1039/D5SC06637A)期刊上。
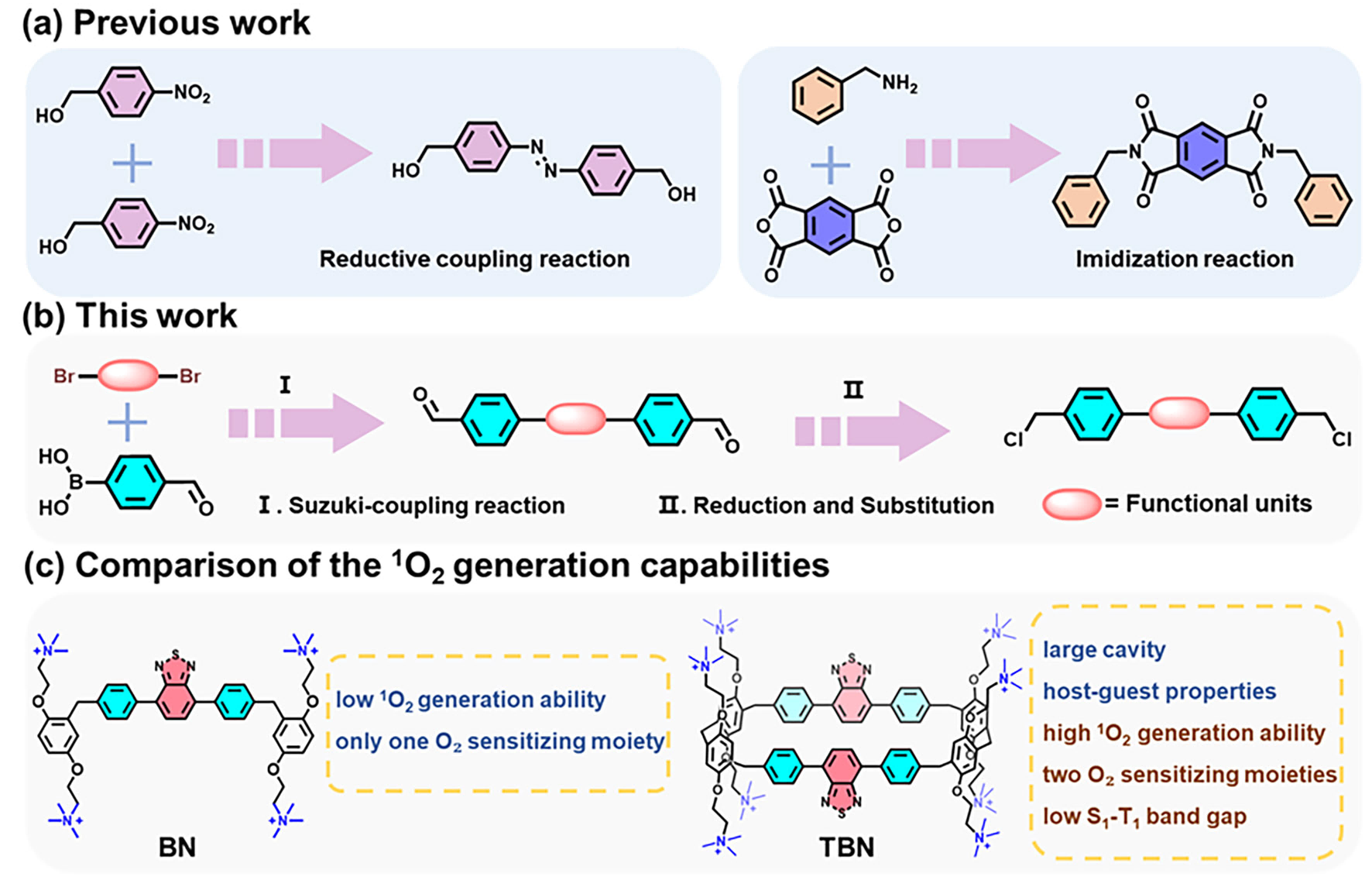
图1.大环分子的结构设计和功能示意图
本研究的创新之处在于其“通用型”的分子设计策略。如图1所示,与传统复杂且受限的合成路线不同,作者开发了一条模块化合成路径,能够将不同的功能单元(如三联苯与苯并噻二唑)精准地嵌入大环化合物的骨架中。通过这一设计,作者成功合成了两类新型大环,即[2]Tp-ExP6和荧光更强的[2]TpB-ExP6。更重要的是,该策略为侧链功能化修饰提供了广阔空间,使得最终制备出水溶性强且带正电的季铵盐功能化大环TBN成为可能,并为后续的抗菌应用奠定了坚实的结构基础。
作者采用9,10-蒽二基-双(亚甲基)二丙二酸(ABDA)作为探针,检测大环分子在光照下的单线态氧生成能力(图2)。结果显示,水溶性大环TBN具备高效的单线态氧生成活性,其单线态氧生成效率远高于非环状前体分子BN。理论计算揭示了大环结构能够减小分子的单重态-三重态能隙,从而更高效地将光能转化为化学能,促进单线态氧的产生。该研究结果表明,精巧的大环分子设计有助于开发具有光动力治疗潜力的新型功能化合物。
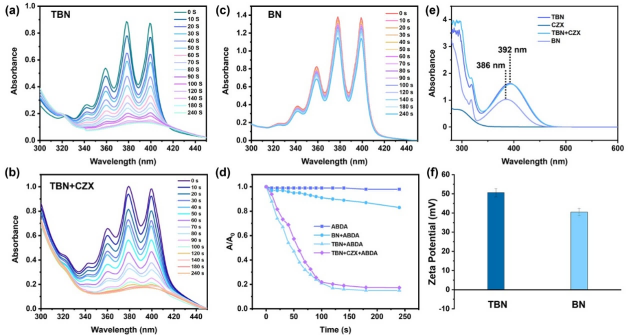
图2.大环TBN和非环前体BN的单线态氧生成能力研究
优异的性能最终需要在实际应用中得到验证。图3所示的抗菌实验结果展现了大环分子TBN在成像与治疗一体化方面的巨大潜力。流式细胞分析和荧光显微成像首先证实了TBN可以靶向并标记细菌(如大肠杆菌和金黄色葡萄球菌)。随后,作者将TBN与抗生素头孢唑肟钠(CZX)联合使用。在光照下,该复合物对多种细菌(包括耐药菌MRSA)都展现出显著的抑菌和清除效果,其最低抑菌浓度在光照下显著降低,菌落几乎被完全清除。这种高效抗菌活性源于TBN的生物膜破坏作用、光动力产生活性氧与抗生素化学杀菌之间的协同效应,为应对耐药菌感染提供了新策略。
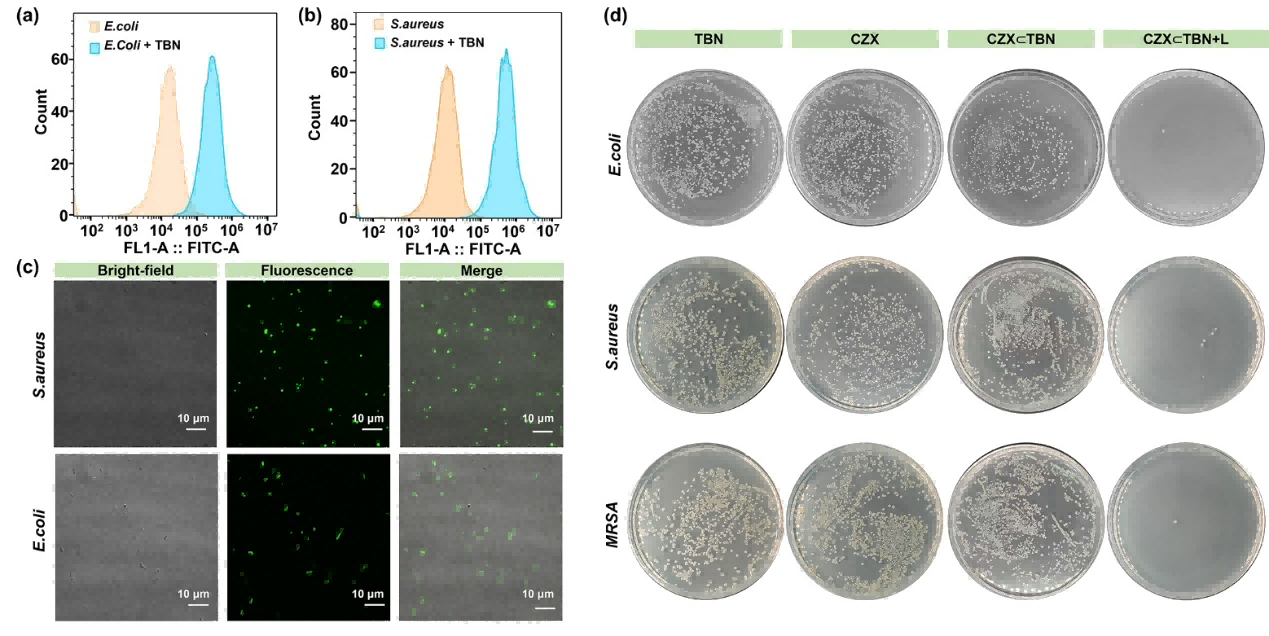
图3.大环TBN的抗菌及成像研究
这项研究通过精准的分子设计,成功实现了识别、成像与治疗功能在单一大环化合物中的集成,为开发新一代智能型抗菌材料提供了全新的设计范式。文章第一作者为海角社区
在读博士研究生刘奥,通讯作者为海角社区
杨英威教授、天津工业大学高辉教授以及海角社区
中日联谊医院王鑫副教授。相关内容已获中国发明专利授权(专利号:ZL202510533737.8)。
论文链接://doi.org/10.1039/D5SC06637A